Nýlega samþykkti kínverska matvæla- og lyfjaeftirlitið (SFDA) opinberlega markaðssetningu tafolecimab (PCSK-9 einstofna mótefni sem er framleitt af INNOVENT BIOLOGICS, INC), INC til meðferðar á frumkólesterólhækkun (þ. kólesterólhækkun) og blandað blóðfituhækkun.Þetta er fyrsti sjálfframleiddi PCSK-9 hemillinn sem sækir um markaðssetningu í Kína.
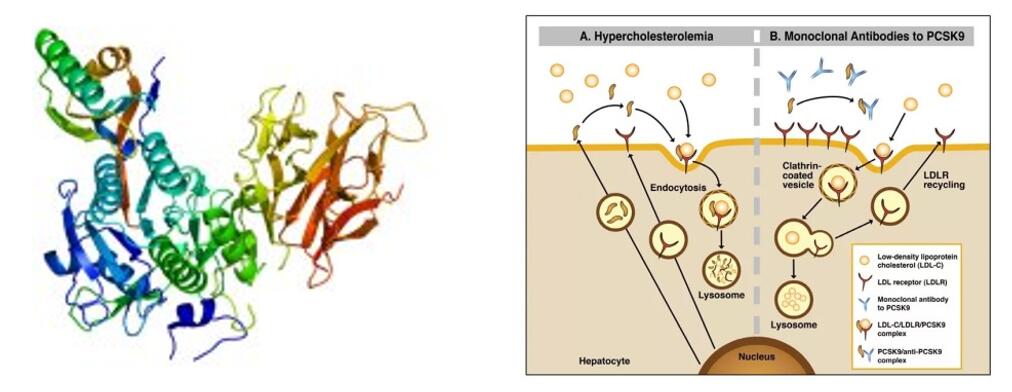
Tafolecimab er nýstárlegt líffræðilegt lyf sjálfstætt þróað af INNOVENT BIOLOGICS, INC. IgG2 manna einstofna mótefni binst PCSK-9 sérstaklega til að auka LDLR gildi með því að draga úr PCSK-9 miðlaðri innfrumumyndun og eykur þar með brotthvarf LDL-C og lækkar LDL-C gildi.
Undanfarin ár hefur algengi blóðfitufalls aukist verulega í Kína.Algengi blóðfituhækkunar og kólesterólhækkunar hjá fullorðnum er allt að 40,4% og 26,3% í sömu röð.Samkvæmt 2020 skýrslunni um hjarta- og æðaheilbrigði og sjúkdóma í Kína er meðferðar- og eftirlitshlutfall blóðfituhækkunar hjá fullorðnum enn á lágu stigi og LDL-C fylgihlutfall blóðfitusjúklinga er enn minna viðunandi.
Áður voru statín aðalmeðferð við kólesterólhækkun í Kína, en mörgum sjúklingum tókst samt ekki að ná meðferðarmarkmiðinu um lækkun LDL-kólesteróls eftir meðferð.Markaðssetning PCSK-9 hefur fært sjúklingum betri virkni.
Skil á tafolecimab frá INNOVENT BIOLOGICS, INC byggist á niðurstöðum þriggja klínískra rannsókna sem skráðar eru á lýðræðislegu stigi, það hefur gott heildaröryggissnið, svipað og öryggiseiginleika markaðssettra vara, og hefur náð langt millibili (á 6 vikna fresti) stjórnsýslunnar.Niðurstöður CREDIT-2 rannsóknarinnar voru samþykktar af 2022 ársfundi American College of Cardiology (ACC) sem ágrip og birtar á netinu.
Ef umsóknin verður samþykkt mun hún rjúfa stöðnun hins innkallaða PCSK-9, Kína verður fjórða landið sem hefur PCSK-9 á eftir Bandaríkjunum (Amgen), Frakklandi (Sanofi) og Sviss (Novartis).
Pósttími: júlí-04-2022